高二英语周报22答案

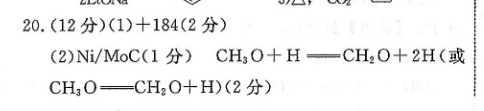


20.(12分)(1)+184(2分)(2)Ni/MoC(1分)CH3O+H=CH2O+2H(或CH3O=CH2O+H)(2分)(3)①低温(1分×(1.9p)2(2分)38(4)大于(2分)水汽转化(2分)解析】(1)△H1=反应物总键能一生成物总键能=3×415kJ·mol-1+462kJ·mol-1+351kJ·mol-l+2×462k·mol-1-2×745kJ·mol-1-3436kJ·mol-l=+184kJ·mol-1。(2)由能量图可知,催化剂N/MoC在该历程中的最大能垒为-0.95eV-(-1.68eV)=0.73eV,催化剂MoC在该历程中的最大能垒为-1.60eV(-2.901.30eV,Ni/MoC催化活性更高,该历程中决定反应速率的步骤的方程式为CH3O+H一CH2O+2H或CH3O=CH2O+H。(3)①由图像可知,随着温度升高CO的选择性增加,CO2的选择性降低,故催化剂在低温区有利于反应i的发生。②由图可知,T=230℃,甲醇的平衡转化率为90%CO的选择性接近于零,故忽略副反应‖的发生,设起始时n(CH3OH)=n(H2O)=amol,列“三段式”:CH3 OH(g)+H2 O(g)CO2(g)+3H2(g)的发生。②由图可知,T=230℃,甲醇的平衡转化率为90%CO的选择性接近于零,故忽略副反应的发生,设起始时n(CH3OH)=n(H2O)=amol,列“三段式”:CH3 OH(g)+H2 O(g)=CO2(g)+3H2(g)起始/mola转化/mol0.9a0.9a2.7平衡/mol0.1a0.10.9a平衡时各组分的物质的量分数为x(CH3OH)z(H2O)=3,x(H1)=33,x(CO2)=3,恒温恒容体系,压强之比等于物质的量之比,起始时n=2amol,对应压强为p,平衡时n=3.8amol,对应压强为1.9力则K38)×。×(1.9p0)2(4)由图像可知,随着水醇比的增加,甲醇的转化率增加,氢气的产率增加,CO的含量降低,故应控制的适宜水醇比大于1:1;随水醇比增加氢气产率的增大趋势大于甲醇转化率的增大趋势,则说明水含量的增加对水汽转化反应更有利。



21.(本题12分))由题意:a2=4,b2=2,所以a=2因为a2=b2+c2,所以c2=2,c所以e分分分所以椭圆C离心率为,长轴长为4因为直线与椭圆交于AB两点,故△>0,解得k2设互,%),B(x2y),则互22+,巧2+1设AB中点G(50y),则2221,%=k+2=_2互+x2k2+1故6假设存在k和点P(m0,使得△PAB是以P为直角顶点的等腰直角三角形则fPG⊥AB,故k·k所以解得2k2+1又因为∠APB所以PA·PB=0所以〔互-mH)(x2-my)=0,即〔-m)1-m)+y2=0整理得〔2+1xx2+(2-m)(x1+x+m2+4=0所以〔2+n.4m2+4=0代入m整理得k当k=-1时,P点坐标为C,O;当k=1时,P点坐标为(,0此时,△PAB是以P为直角顶点的等腰直角三角形

以上就是高二英语周报22答案,更多英语周报答案请关注本网站。






