2022英语周报HBJ七答案

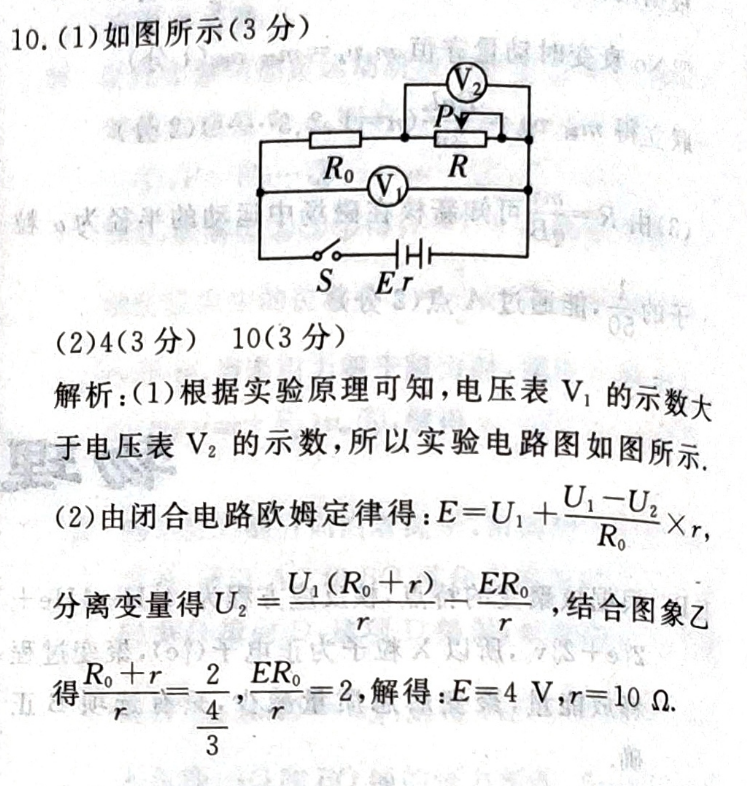
10.(1)如图所示(3分)2RR4洋。一HS E如函(2)4(3分)10(3分)解析:(1)根据实验原理可知,电压表V1的示数大于电压表V2的示数,所以实验电路图如图所示(2)由闭合电路欧姆定律得:E=U1+Rr分离变量得VU1(R0+),结合图象乙午A图,7+。1得R+r2ER=2,解得:E=4V,=10.4

7.(13分)(1)粉碎水钴矿、搅拌、适当升高温度、适当增大硫酸浓度(1分,任答1条即可)(2)SiO2(1分(3)2C3++H2O22C02++O2↑+2H+(2分)Fe3+可以催化H2O2分解(1分)(4)3.2≤pH1<4.5(2分)b(2分)(5)0.042mol·L-1(2分)(6)蒸发浓缩、冷却结晶、过滤(洗涤、干燥)(2分)【解析】(1)“酸浸”时,能提高浸出率的措施有粉碎水钴矿、搅拌、适当升高温度、适当增大硫酸浓度等。(2)混合物中只有SiO2不溶于硫酸,所以滤渣1的主要成分为SO2(3)“还原”的目的是将Co3还原为Co2+,所以发生反应的离子方程式为2Co3++H2O2=2C02++O2↑2H+;所需H2O2的量远高于理论值的原因为Fe3+可以催化H2O2分解(4)“调pH1”的目的为沉淀Fe3+,不沉淀AP+,所以pH1范围为3.2≤pH1<4.5。Fe2O3不能用于沉淀e3+,Na2SO3可将Fe3+还原,可选用氨水沉淀Fe故选b。(5)沉淀c(Mg2+)=0.02mol·L-溶液中的Mg2+需要c(F-)=0.04mol·L-;要保持溶液中c(Mg2+)不高于1.0×10-5mol·L-,根据K(MgF2)=110-1,可知需要保持反应后溶液中c(F-)不低于0.001mol·L-,故所加NaF溶液的物质的量浓度应不低于0.042mol·L(6)从溶液中得到结晶水合物的方法为蒸发浓缩、冷却结晶、过滤(洗涤、干燥)。

以上就是2022英语周报HBJ七答案,更多英语周报答案请关注本网站。






